Applicazioni del
coefficiente economico e del coefficiente economico della macchina di Carnot
Il calore utilizzato come
fonte energetica convertibile in lavoro, nella maggior parte dei casi, è
prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate
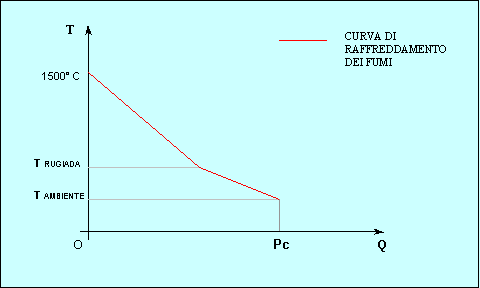
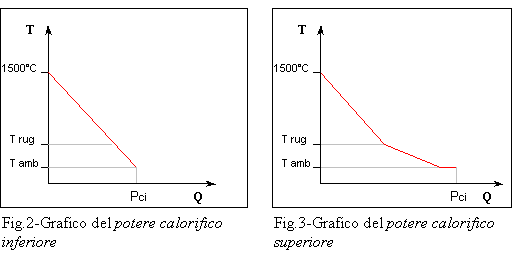
combustibili. In particolare, la grandezza fisica che permette di quantificare
l’energia da essi prodotta è il potere calorifico; ma per comprendere meglio
questo concetto, è necessario prima di tutto chiarire le varie fasi del
processo di combustione.
Supponiamo di avere un combustibile di massa
pari ad 1 kg. Esso è chimicamente composto da alcune sostanze, dette ossidabili, che, combinandosi con una
certa quantità di ossigeno (O2),
innescano il processo di combustione. Tale massa O2 è genericamente indicata con N kg (dove N>1) poiché può variare a seconda dei combustibili
impiegati, ognuno dei quali, sottoponendo diverse quantità di reagenti,
richiede di conseguenza diverse quantità di ossigeno.
I prodotti della
combustione saranno principalmente due: l’anidride carbonica (CO2) e
l’acqua (H2O).
Inoltre,è importante
notare che nel processo non si ha a disposizione ossigeno allo stato puro, ma
aria, che, oltre al 20% di O2 contiene un’alta percentuale di azoto (N2).
Di conseguenza, nella reazione viene trascinata una quantità M kg di tale elemento, che aumenta la
massa dei fumi, ma non prende parte attivamente alla combustione.
Il procedimento complessivo si può così riassumere:
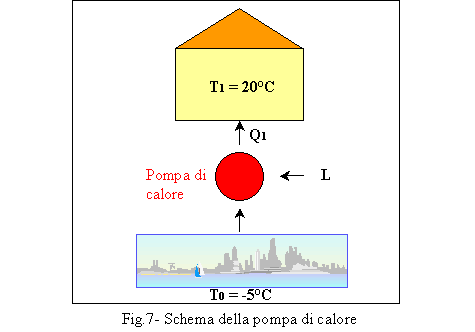
Si supponga ora di voler
riscaldare un’abitazione alla temperatura di 20°C, quando l’ambiente esterno è
a 5°C.
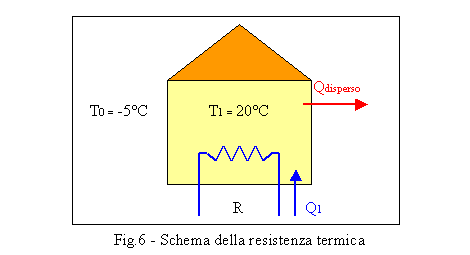
L’involucro della casa
tende a disperdere una certa potenza termica; quindi, affinché la temperatura
interna rimanga a 20°C, è importante assicurare l’apporto di una quantità di
calore Q1, uguale e contraria a quella dissipata.
Volendo ipotizzare un
calcolo semplice poniamo tale flusso di calore pari a un kw (Q1 = 1
kw).
A questo punto ci sono due alternative
possibili per fornire questo calore all’abitazione:
-tramite una resistenza
elettrica
-tramite una pompa di
calore.
Resistenza elettrica:
consiste
nell’applicazione di un generatore di corrente. La potenza elettrica è uguale
alla quantità di calore che è necessario fornire.
Q1 = L = 1kw
![]()
Trattandosi di una
macchina reversibile posso calcolare il coefficiente economico della macchina
di Carnot:
![]()
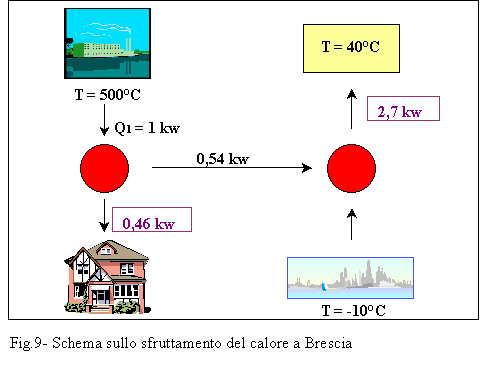
quindi
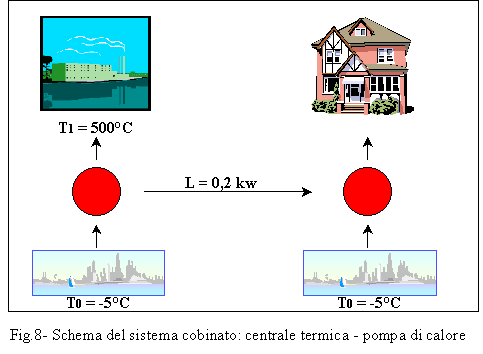
bruciando 1 kw di combustibile, il 54% viene utilizzato per vari scopi, mentre
il restante 46%, invece di essere espulso nell’ambiente, come già abbiamo
accennato precedentemente, viene recuperato ed inviato alle varie abitazioni.
Un
modo utile per verificare l’efficienza di tale riscaldamento è espresso dal CUC
definito come l’energia ottenuta diviso l’energia spesa:
![]()